Autophagy |公共卫生学院(深圳)孙彩军教授团队成功研发一种靶向自噬信号通路的新型广谱流感疫苗策略
近日,中山大学公共卫生学院(深圳)孙彩军教授团队在国际学术期刊《Autophagy》在线发表了一项研究成果,题为"Redirecting neuraminidase antigen to autophagosomes confers enhanced cross-reactive T cell immunity against heterosubtypic influenza virus infection”。
流感是全球公共卫生领域的重大挑战,而疫苗接种被认为是最具成本效益的防控手段。神经氨酸酶(NA)是流感病毒表面仅次于血凝素(HA)的第二丰富的膜蛋白,其头部包含高度保守的酶活性位点且抗原漂移速率更慢,因此NA具有成为新型流感疫苗靶标的潜力。然而,天然形式NA蛋白的免疫原性较弱,目前的灭活流感疫苗在人体内对NA的血清转化率仅为30%左右。因此,提升其免疫原性是研发NA靶向流感疫苗的关键科学问题。为突破这一瓶颈,中山大学公共卫生学院(深圳)孙彩军教授团队创新性地提出将NA抗原导向细胞自噬通路以增强其免疫原性的策略。
研究团队首先构建了表达NA与自噬体标记物LC3B融合蛋白的重组DNA疫苗和复制缺陷型VSV载体疫苗,结果显示NA-LC3B融合蛋白能被有效招募至自噬体-溶酶体-MHC II抗原提呈通路。研究还发现,自噬诱导剂可降低NA-LC3B蛋白水平,而自噬阻断剂则导致其积累,证实该融合蛋白确实经由自噬-溶酶体途径降解。接着,采用DNA初免-VSV载体加强的免疫策略,在小鼠模型中评估了NA-LC3B疫苗的免疫原性。结果显示该疫苗有效诱导了NA特异性IgG抗体(倾向于Th1型的IgG2a抗体),且产生了强烈的NA特异性细胞免疫应答,而传统裂解苗组几乎检测不到NA特异性T细胞应答。更重要的是,面对致死剂量的同源H1N1病毒攻击,NA、NA-LC3B和裂解苗免疫组小鼠均获得100%保护;而当面对异亚型H3N2病毒攻击时,裂解苗组全部死亡,而NA-LC3B组则将存活率显著提升至60%。
为探索交叉保护的免疫机制,研究者合成了覆盖NA全长序列的92条15氨基酸多肽片段,并将其分为20个亚库,通过二维矩阵扫描策略系统筛选T细胞应答谱。该研究中不仅验证了已知免疫优势表位,还新鉴定出24条NA特异性T细胞表位,其中多个为首次报道。与NA相比,NA-LC3B显著拓宽了T细胞应答谱,额外诱导出4个新的CD4+T细胞表位和4个新的CD8+T细胞表位。序列比对分析表明,部分新表位在H1N1与H3N2亚型间同源性超过90%,这为理解其交叉保护能力提供了分子基础。研究团队进一步在免疫小鼠中进行了T细胞清除实验,结果显示清除CD4+和CD8+T细胞后再进行攻毒,NA-LC3B组的存活率由100%降至40%,且存活小鼠体重显著下降。这直接证明NA-LC3B疫苗提供的保护力主要依赖于其激发的T细胞免疫。
综上所述,该研究通过将NA抗原导向自噬通路,成功开发出一种能够激发强效、广谱、多功能T细胞免疫的新型广谱流感疫苗策略。这种抗原设计思路也为其他病毒疫苗和肿瘤免疫治疗开辟了新方向。目前,该疫苗策略已获得中国发明专利授权。
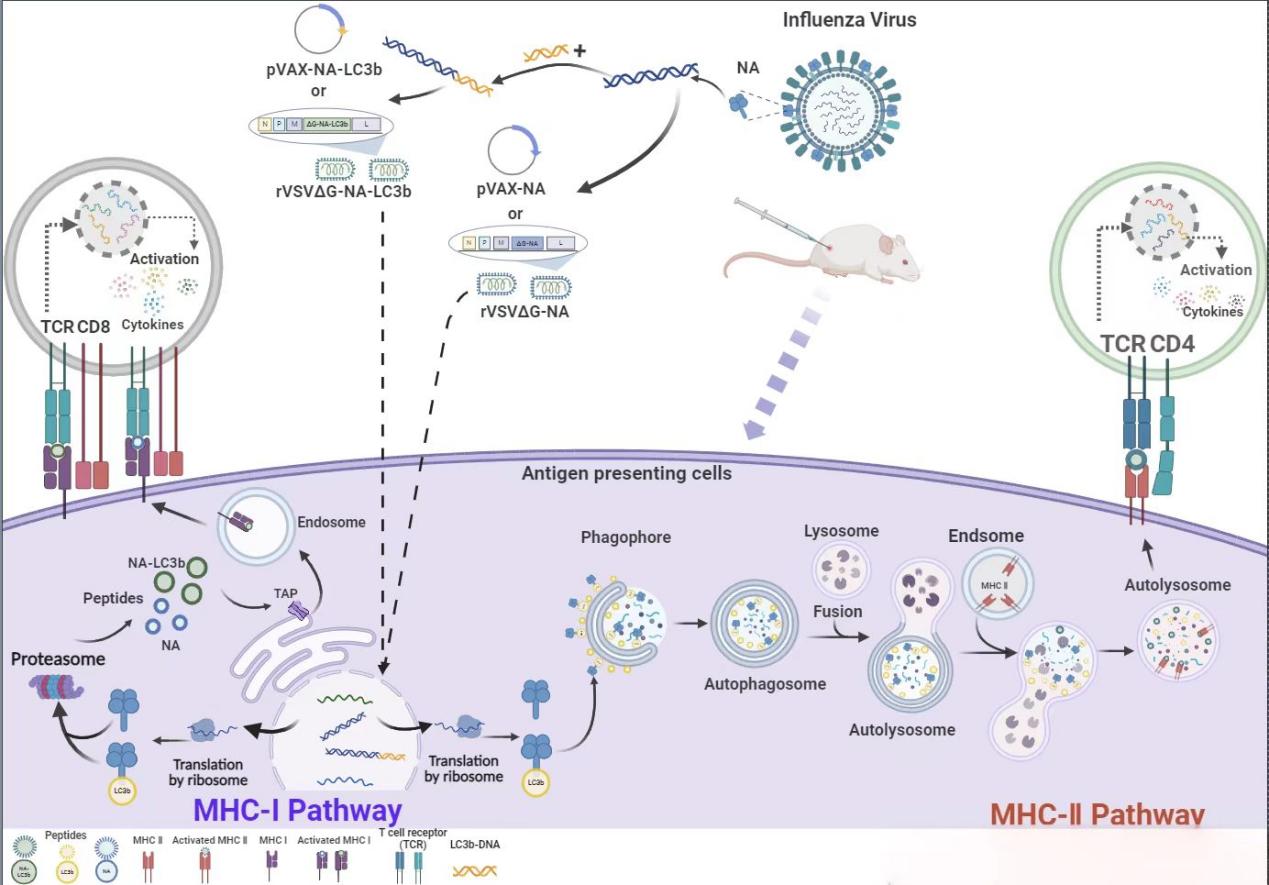
图1 靶向自噬信号通路的增强型流感疫苗策略摘要图
中山大学为论文完成第一单位,孙彩军教授、舒跃龙教授和陈耀庆教授为共同通讯作者,韩子蓉博士、潘蔚琦研究员、赖文龙博士为共同第一作者。该研究获得国家重点研发计划(2022YFC2304204)、国家自然科学基金(82271786)、广东省科技计划项目(2021B1212040017)等项目资助,还得到深圳康泰生物制品股份有限公司和云舟生物科技(广州)股份有限公司的支持。
据悉,孙彩军团队近期合作研发出一系列可诱发广谱免疫应答的流感疫苗抗原设计和递送系统新策略(Autophagy, 2026;Virol Sin., 2026;J Virol. 2025; RNA, 2025; Vaccine,2025;EBioMedicine. 2024;NPJ Vaccines. 2024;Int J Biol Macromol. 2024;Antiviral Res. 2024;npj Vaccines. 2023)。
论文链接:
https://www.tandfonline.com/doi/full/10.1080/15548627.2026.2629285
撰稿:孙彩军课题组
初审:何嘉敏
审核:孙力涛
审核发布:汪宗芳


